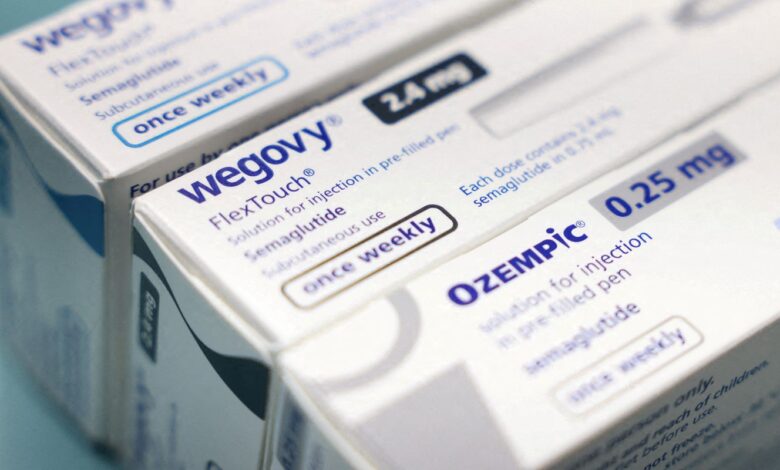
Brasília — InkDesign News — A Agência Nacional de Vigilância Sanitária (Anvisa) proibiu a manipulação da substância semaglutida, utilizada em canetas de emagrecimento como Ozempic e Wegovy, estabelecendo novas diretrizes para a importação e manipulação de insumos farmacêuticos ativos.
Contexto e objetivos
A semaglutida é um agonista do hormônio GLP-1, amplamente utilizado no tratamento de diabetes tipo 2 e obesidade. Com a recente decisão, a Anvisa visa proteger a saúde da população brasileira, especialmente contra produtos manipulados que não garantem a segurança e eficácia necessárias. O público-alvo dessa regra abrange pacientes que necessitam de tratamentos adequados e seguros para condições metabólicas.
Metodologia e resultados
A determinação da Anvisa afirma que insumos biotecnológicos, como a semaglutida, podem ser importados somente se forem do mesmo fabricante registrado no Brasil, restringindo a manipulação apenas a produtos devidamente autorizados. “Por exemplo, atualmente, a semaglutida possui registro apenas como produto biotecnológico. Portanto, não é permitida a importação nem a manipulação da semaglutida sintética até que exista um medicamento registrado com o IFA sintético”, explicou a agência.
A proibição visa, essencialmente, eliminar o risco de medicamentos irregulares que podem prejudicar os pacientes.
(“Medicamentos irregulares não oferecem garantia de pureza, dosagem correta, estabilidade ou esterilidade, podendo resultar em ineficácia do tratamento, reações adversas graves e contaminação, colocando a saúde e segurança do paciente em risco.”)— Nota da Novo Nordisk.
Implicações para a saúde pública
O impacto dessa decisão se estende à segurança dos tratamentos disponíveis no mercado. A Sociedade Brasileira de Endocrinologia e Metabologia (SBEM) considera essa proibição vital para evitar riscos à saúde pública. A SBEM argumenta que os mesmos riscos associados à manipulação da semaglutida são aplicáveis à tirzepatida, outra substância utilizada no tratamento de obesidade e diabetes. Assim, a entidade solicitou que a Anvisa institua uma proibição semelhante à tirzepatida, levando em conta os possíveis perigos que a manipulação desse medicamento pode trazer aos pacientes.
A manutenção de uma proibição parcial, restrita apenas à semaglutida, abre espaço para a migração do mercado irregular para a tirzepatida manipulada, perpetuando o risco sanitário e expondo pacientes a produtos inseguros.
(“A SBEM solicitou formalmente que a Anvisa estenda a medida cautelar também à tirzepatida, proibindo sua manipulação em território nacional.”)— SBEM.
A decisão da Anvisa, portanto, abre espaço para a prevenção de práticas que possam comprometer a saúde da população e reforça a importância de garantir tratamentos que atendam a protocolos rigorosos de segurança e eficácia.
Fonte: (Agência Brasil – Saúde)